Páginas
▼
viernes, 27 de abril de 2018
Síndrome urémico-hemolítico
Caso clínico: Una mujer de 33 años y su hijo de 5 años acudieron al servicio de urgencias por presentar diarrea sanguinolenta y dolor abdominal difuso. La mujer refiere que la sintomatología diarreica apareció 24 horas después de haber consumido carne de res poco cocida y una hamburguesa para el niño en un restaurante no muy conocido, y que unos días después aparecieron sangre en las heces en los dos pacientes. Fueron hospitalizados para valoración y los exámenes complementarios mostraron que la diarrea no era inflamatoria. La mujer mejoró satisfactoriamente; sin embargo, al cuarto día de hospitalización, el niño presentó insuficiencia renal aguda. Los exámenes de sangre evidenciaban disminución en las plaquetas y anemia hemolítica.
a. Cuál es la bacteria involucrada en la infección de éstos dos pacientes?
i. Campylobacter jejuni
ii. Shigella dysenteriae
iii. E. coli entero invasiva
iv. E. coli entero hemorrágica
b. Cuál es el mecanismo de acción del factor de virulencia involucrado?
El síndrome urémico-hemolítico (SUH) esta causado por las gastroenteritis provocadas por E. coli entero-hemorrágica, Shigella dysenterie tipo I, Campylobacter yeyuni, Yersinia, Salmonella sp.)
Está causado por una exotoxina tipo Shiga (Stx) producida por la Shigella dysenteriae tipo 1, la E. coli entero hemorrágico productor de la toxina Shiga es llamado STEC, existiendo varios tipos de Stx: Stx1, Stx2, Stx2c, Stx2d, Stx2e, Stx2f, Stx2g y Stx2h; estas Stx están compuestas por una subunidad central A, que posee una acción inhibitoria sobre la síntesis proteica ribosomal con inducción de apoptosis y cinco unidades B, una de las cuales permite la adherencia a receptores específicos de naturaleza glicolipídica Gb3 (globotriosilceramida) presentes en las membranas de los endotelios vasculares, especialmente de los glomérulos y de las células de los túbulos proximales de los riñones donde causan lesiones en las membranas y en las células y secundariamente trombosis; a nivel del SNC Stx produce lesiones directas de las neuronas, de los oligodendrocitos y de los astrocitos de tipo degenerativo en diferentes áreas del cerebro.
Ejercicios de bacteriología
Caso clínico: Un bombero severamente quemado, se encuentra hospitalizado, después de varios días de estadía, empezó a desarrollar una infección generalizada en las heridas con presencia de "pus verdosa". Se envía una muestra de la secreción de una de las heridas al laboratorio evidenciándose bacilos Gram negativos, oxidasa-positivos. ¿Qué enunciado es correcto respecto al agente causa más probable?
Se trata de Pseudomonas aeruginosa, un bacilo Gram negativos no fermentador, que tienen un metabolismo oxidativo, por eso son oxidasa positivos.
Varios días de estadía en hospital... se supone que ha estado en tratamiento antibiótico sin que remita la infección. El pus verdoso es debida a la pioverdina.
------------------------------------------------------------------------------------------------------------------
Caso clínico: En un paciente con dolor insoportable de la espalda baja, son sintomatología urinaria, se realizó un cultivo de orina en la cual se identificaron enterobacterias no fermentadoras. Un urograma excretor detectó la presencia de cálculos renales. ¿Cuál es el mecanismo de acción para desarrollar cálculos renales?
Casi el 80% de los cálculos renales están compuestos de oxalato de calcio. Otros tipos de cálculos más raros se componen de: cistina (un aminoácido que se encuentra en alta concentración en las personas con cistinuria), ácido úrico u otras sustancias.
Los cálculos también pueden estar compuestos por estruvita (magnesio, amonio y fosfato) en un 10% de los casos. La formación de cálculos de estruvita se asocia con la presencia de una bacteria (Klebsiella, Serratia, Proteus, especies de Providencia) que convierte la urea en amoníaco. La bacteria implicada más común es la Proteus mirabilis. Casi el 40% de los cálculos tienen varios compuestos en la misma piedra. Proteus mirabilis tiene la habilidad de producir grandes niveles de ureasa. La ureasa hidroliza urea a amoníaco, (NH3) y eso hace a la orina más alcalina. Y al subir la alcalinidad precipita el carbonato cálcico y la estruvita.
-------------------------------------------------------------------------------------------------------------------
Caso clínico: Mujer de 25 años de edad, acudió a la consulta médica por presentar dolor pelvico y ardor al orinar, frecuencia, disuria, fiebre baja. El cultivo de orina evidenció la presencia de bacilos Gram negativos, oxidasa negativos, fermentadores. Pensando en la bacteria más frecuentemente asociada a estas infecciones:
a. ¿Qué factor de virulencia es necesario para que la bacteria establezca la infección? Fimbrias. Posteriormente pueden invadir las células epiteliales de la vejiga escapando así a la acción de los macrófagos
b. ¿Qué bacteria puede ser la responsable? E. coli uropatogenica
La cistitis es una inflamación de la vejiga que causa una sensación de ardor al orinar, sangre en la orina, dolor, fiebre u otros síntomas. Es una enfermedad común en las mujeres, pero también se puede presentar en los hombres. Un 30% de las mujeres sufrirán un episodio de cistitis a lo largo de su vida. La causante es E. coli, responsable del 85 por ciento de las infecciones no complicadas en mujeres sexualmente activas. Estos gérmenes se encuentran en el intestino y contagian a través de las heces (enterobacterias). También puede producirse por tricomonas, Chlamidias, Proteus y Klebsiella.
Caso clínico: Un hombre de 60 años que recibió un transplante de hígado 5 años antes de su ingreso hospitalario para volorar un cuatdro de dolor abdominal espasmódico y diarrea intensa. Tres semanas antes de su ingreso había recibido un ciclo de 10 días de duración con trimetoprima-sulfametoxazol por vía oral por una sinusitis. A la exploración física el paciente estaba febril con una palpación moderadamente dolorosa en el abdomen. La tomografía computerizada reveló un engrosamiento del colon derecho sin abscesos. La colonoscopia puso de manifiesto numerosas placas blanquecinas con una mucosa eritematosa compatible con colitis pseudomembranosa. ¿Qué bacteria puede estar implicada? Razona tu respuesta.
Se trata de una infección por Clostridium difficile. Es muy significativo que el paciente recibiera tratamiento con antibióticos durante 10 días previamente. Este tratamiento eliminó su flora intestinal permitiendo que sus esporas resistiesen el tratamiento y germinando al acabar el ciclo de antibióticos. El rápido crecimiento de Clostridium permitió a la bacteria colonizar el colon en poco tiempo. La colitis pseudomembranosa es característica de esta bacteria.
Caso clínico: Un paciente hospitalizado por dos meses debido a una fractura expuesta complicada con una infección, empezó desde hace una semana con sintomatología sistémica, fiebre alta, malestar general, escalofríos. Los antibióticos no han mejorado e estado de salud, un cultivo de sangre demostró la presencia de bacilos Gram negativos, oxidasa positivos. El examen físico ha demostrado el aparecimiento de lesiones hemorrágicas y necróticas en la piel. Usted sospecha de ectima gangrenoso.
Pseudomonas aeruginosa puede causar una infección en la piel llamada ectima gangrenoso. Se presenta como una lesión redonda u oval, de entre 1 y 15 cm de diámetro, con un halo eritematoso. Habitualmente, aparece un centro necrótico rodeado por una zona eritematosa, que representa el lugar en el que el microorganismo ha invadido los vasos sanguíneos produciendo pequeños infartos en la piel. El mecanismo de destrucción del tejido se produce por la exotoxina A. Esta toxina es similar a la toxina del Corynebacterium diphteriae su modo de acción es bloqueando la síntesis de proteínas en el ribosoma y provocando la muerte celular
Se trata de Pseudomonas aeruginosa, un bacilo Gram negativos no fermentador, que tienen un metabolismo oxidativo, por eso son oxidasa positivos.
Varios días de estadía en hospital... se supone que ha estado en tratamiento antibiótico sin que remita la infección. El pus verdoso es debida a la pioverdina.
------------------------------------------------------------------------------------------------------------------
Caso clínico: En un paciente con dolor insoportable de la espalda baja, son sintomatología urinaria, se realizó un cultivo de orina en la cual se identificaron enterobacterias no fermentadoras. Un urograma excretor detectó la presencia de cálculos renales. ¿Cuál es el mecanismo de acción para desarrollar cálculos renales?
Casi el 80% de los cálculos renales están compuestos de oxalato de calcio. Otros tipos de cálculos más raros se componen de: cistina (un aminoácido que se encuentra en alta concentración en las personas con cistinuria), ácido úrico u otras sustancias.
Los cálculos también pueden estar compuestos por estruvita (magnesio, amonio y fosfato) en un 10% de los casos. La formación de cálculos de estruvita se asocia con la presencia de una bacteria (Klebsiella, Serratia, Proteus, especies de Providencia) que convierte la urea en amoníaco. La bacteria implicada más común es la Proteus mirabilis. Casi el 40% de los cálculos tienen varios compuestos en la misma piedra. Proteus mirabilis tiene la habilidad de producir grandes niveles de ureasa. La ureasa hidroliza urea a amoníaco, (NH3) y eso hace a la orina más alcalina. Y al subir la alcalinidad precipita el carbonato cálcico y la estruvita.
-------------------------------------------------------------------------------------------------------------------
 |
| Diferencias entre Salmonella y Shigella: |
 |
| Distintas morfologías celulares bacterianas |
a. ¿Qué factor de virulencia es necesario para que la bacteria establezca la infección? Fimbrias. Posteriormente pueden invadir las células epiteliales de la vejiga escapando así a la acción de los macrófagos
b. ¿Qué bacteria puede ser la responsable? E. coli uropatogenica
La cistitis es una inflamación de la vejiga que causa una sensación de ardor al orinar, sangre en la orina, dolor, fiebre u otros síntomas. Es una enfermedad común en las mujeres, pero también se puede presentar en los hombres. Un 30% de las mujeres sufrirán un episodio de cistitis a lo largo de su vida. La causante es E. coli, responsable del 85 por ciento de las infecciones no complicadas en mujeres sexualmente activas. Estos gérmenes se encuentran en el intestino y contagian a través de las heces (enterobacterias). También puede producirse por tricomonas, Chlamidias, Proteus y Klebsiella.
Caso clínico: Un hombre de 60 años que recibió un transplante de hígado 5 años antes de su ingreso hospitalario para volorar un cuatdro de dolor abdominal espasmódico y diarrea intensa. Tres semanas antes de su ingreso había recibido un ciclo de 10 días de duración con trimetoprima-sulfametoxazol por vía oral por una sinusitis. A la exploración física el paciente estaba febril con una palpación moderadamente dolorosa en el abdomen. La tomografía computerizada reveló un engrosamiento del colon derecho sin abscesos. La colonoscopia puso de manifiesto numerosas placas blanquecinas con una mucosa eritematosa compatible con colitis pseudomembranosa. ¿Qué bacteria puede estar implicada? Razona tu respuesta.
Se trata de una infección por Clostridium difficile. Es muy significativo que el paciente recibiera tratamiento con antibióticos durante 10 días previamente. Este tratamiento eliminó su flora intestinal permitiendo que sus esporas resistiesen el tratamiento y germinando al acabar el ciclo de antibióticos. El rápido crecimiento de Clostridium permitió a la bacteria colonizar el colon en poco tiempo. La colitis pseudomembranosa es característica de esta bacteria.
 |
| Colitis pseudomembranosa por Clostridium difficile. Fuente |
Pseudomonas aeruginosa puede causar una infección en la piel llamada ectima gangrenoso. Se presenta como una lesión redonda u oval, de entre 1 y 15 cm de diámetro, con un halo eritematoso. Habitualmente, aparece un centro necrótico rodeado por una zona eritematosa, que representa el lugar en el que el microorganismo ha invadido los vasos sanguíneos produciendo pequeños infartos en la piel. El mecanismo de destrucción del tejido se produce por la exotoxina A. Esta toxina es similar a la toxina del Corynebacterium diphteriae su modo de acción es bloqueando la síntesis de proteínas en el ribosoma y provocando la muerte celular
 |
| Ectima gangrenoso provocado por Pseudomonas aeruginosa. Fuente |
jueves, 26 de abril de 2018
¿Diarrea del viajero por Gram positivos?
Caso clínico: Una
paciente alemana de 19 años se encuentra de visita en el Ecuador
desde hace tres semanas de intercambio. No ha viajado fuera de la
provincia de Pichincha, pero ha consumido alimentos en lugares de
expendio de alimentos como FoodTracks. El cultivo de heces demostró
ser un bacilo Gram positivo, la bacteria creció en medios para
aislamiento de enterobacterias.
Las preguntas de exámenes son para razonar. Muchas veces algún dato no cuadra. La vida no es perfecta. Si usas un medio selectivo para enterobacterias Gram negativas como el agar MacConkey, se te puede colar alguna Gram positiva por ejemplo, Enterococcus o algunas Staphylococcus. Enterococcus son muy resistentes a condiciones adversas (congelación,
desecación, tratamiento térmico, etc.) por lo que son buenos indicadores
para valorar las condiciones higiénicas y de conservación de los
alimentos congelados y desecados, por lo que podría ser en este caso clínico.
El medio de selección de enterobacterias es usualmente agar MacConkey, contiene sales biliares y cristal violeta, que son medios inhóspitos para que crezcan las enterobacterias.
Los ingredientes del MacConkey son los siguientes:
Sales biliares
Colorante cristal violeta (inhóspito para cierto tipo de bacterias Gram-positivo),
Indicador rojo neutro (el cual marca microorganismos que fermenten la lactosa),
Lactosa
Peptona (básicamente un caldo de carne donde las proteínas están degradadas como lo podrían estar en el intestino)
Cloruro sódico.
El indicador rojo neutro marca microorganismos que fermenten la lactosa. Sirve como un indicador visual de pH, distinguiendo así las bacterias Gram negativas que pueden fermentar la lactosa (Lac+) y las que no pueden (Lac-).
Lac+
Al utilizar la lactosa en el medio, las bacterias Lac+ como lo son Escherichia coli, Enterobacter y Klebsiella producen acidez, lo cual hace que baje el pH de 7,1 ± 0,2 lo que tiene como consecuencia la aparición de colonias de color rosadas o rojas. Algunas bacterias en cambio fermentan la lactosa de manera lenta, estas siguen siendo Lac+ por ejemplo: Serratia y Citrobacter.
Lac- Bacterias que no fermenten la lactosa como lo son Salmonella, Proteus y Shigella utilizaran peptona en su lugar, formando amoníaco, lo cual incrementa el pH del agar, formando colonias blancas o incoloras.
Si la bacteria no fuese una Gram positiva ¿Cuál es el agente etiológico más probable en este caso de diarrea?
Como este caso clínico se corresponde a una diarrea del viajero la respuesta correcta sería E. coli enterotoxigénica. Descartaríamos Vibrio cholerae porque es una diarrea que no ocurre en la costa y tampoco está asociada al consumo de mariscos.
El medio de selección de enterobacterias es usualmente agar MacConkey, contiene sales biliares y cristal violeta, que son medios inhóspitos para que crezcan las enterobacterias.
Los ingredientes del MacConkey son los siguientes:
Sales biliares
Colorante cristal violeta (inhóspito para cierto tipo de bacterias Gram-positivo),
Indicador rojo neutro (el cual marca microorganismos que fermenten la lactosa),
Lactosa
Peptona (básicamente un caldo de carne donde las proteínas están degradadas como lo podrían estar en el intestino)
Cloruro sódico.
Agar MacConkey con colonias Lac+ (izquierda) y colonias Lac- (derecha).
El indicador rojo neutro marca microorganismos que fermenten la lactosa. Sirve como un indicador visual de pH, distinguiendo así las bacterias Gram negativas que pueden fermentar la lactosa (Lac+) y las que no pueden (Lac-).
Lac+
Al utilizar la lactosa en el medio, las bacterias Lac+ como lo son Escherichia coli, Enterobacter y Klebsiella producen acidez, lo cual hace que baje el pH de 7,1 ± 0,2 lo que tiene como consecuencia la aparición de colonias de color rosadas o rojas. Algunas bacterias en cambio fermentan la lactosa de manera lenta, estas siguen siendo Lac+ por ejemplo: Serratia y Citrobacter.
Lac- Bacterias que no fermenten la lactosa como lo son Salmonella, Proteus y Shigella utilizaran peptona en su lugar, formando amoníaco, lo cual incrementa el pH del agar, formando colonias blancas o incoloras.
Si la bacteria no fuese una Gram positiva ¿Cuál es el agente etiológico más probable en este caso de diarrea?
i. E. coli entero
toxigénica
ii. E. coli entero
patogénica
iii. Vibrio cholerae
iv. Vibrio
parahaemolyticus
v. Vibrio vulnificus
Como este caso clínico se corresponde a una diarrea del viajero la respuesta correcta sería E. coli enterotoxigénica. Descartaríamos Vibrio cholerae porque es una diarrea que no ocurre en la costa y tampoco está asociada al consumo de mariscos.
martes, 24 de abril de 2018
La filogenia no tiene sensibilidad para el mestizaje
Cuando leemos sobre Salmonella y Shigela nos encontramos con todo el tema de los serotipos y los biotipos... algo difícil de entender. ¿Por qué antes definíamos a Salmonella typhi, Salmonella choleraesuis, Salmonella typhimurium, Salmonella enteritidis... y ahora las englobamos dentro de Salmonella enterica serovariedad Typhi? La respuesta está en los filogenéticos, personas que analizando genes que varían poco, como los ribosomales 16s realizan árboles familiares (filogenéticos) y han llegado a la conclusión que los 2500 serotipos distintos de Salmonella enterica son una sola especie con serotipos distintos.
El problema, incluso diría el error, está en considerar que podemos hacer árboles filogenéticos basados en ciertas secuencias y no considerar que las bacterias pueden recibir aportes genéticos externos, normalmente plásmidos, transposones... y ese aporte genético les da unas peculiaridades patológicas que las convierten de hecho en especies nuevas. Da igual que el 99.9% de las secuencias genéticas cromosómicas sean similares. Con que una Salmonella, o un E. coli o Shigela (dicen que es un biotipo de E. coli) hayan adquirido genes de patogenicidad y éstos les abran el acceso a nuevos nichos ecológicos ésta nueva presión selectiva hará que se conviertan en especies nuevas. Por eso tradicionalmente a estos serotipos se les han denominado como especies.
Para entender los árboles familiares (filogenéticos) es muy útil emplear un simil linguístico como analogía. Por ejemplo, las lenguas romances como el francés, español, portugués, rumano proceden del latín. Si tomamos una palabra del latín original "factum" podemos ver como ha evolucionado a las palabras de los idiomas romances actuales
Las palabras van a tener un grado de identidad con la palabra "factum" de la cual proceden. Por ejemplo, el inglés tomó la palabra del latín recientemente por ese motivo hay muy poco cambio, de factum a fact. Si consideramos factum como el 100% de identidad, fact tiene 5 letras de las 6 letras originales. Cinco entre seis nos da un 83% de similitud. El castellano actual tiene 1 letra, la c en hecho, de seis de factum, uno dividido entre seis 17%.
Con esos datos, podemos concluir que la palabra fact está más cerca del latín que hecho. Utilizamos el porcentaje de similitud como un mapa. Si dos puntos tienen 17% de similitud, es lo mismo que decir 83% de distancia (100-17). La palabra hecho estaría un 83% alejada de factum. Dos puntos a tan solo 17% de distancia (100-83 similitud) como es el caso de factum y fact indicaría que estarían proximos.
En el caso de hecho, castellano actual, está más próxima a fecho, castellano antiguo, que a feito, palabra galego-portuguesa. De esta manera generamos, lo mismo que cuando comparamos las distancias entre distintas ciudades, un gráfico resumen de la distancia entre las palabras:
Con estas distancias se pueden construir árboles filogenéticos, que curiosamente se pueden superponer a mapas físicos:
Lo curioso es que los señor@s filogenetistas no contemplen que en cada uno de esos territorios hay una historia de mestizaje. Por ejemplo, a pesar de que el castellano deriva en su mayor parte del latín, no podemos hacer una historia genealógica común con el término izquierdo, que es de origen íbero. Tendríamos que remontarnos mucho más atrás, a las lenguas indoeuropeas para encontrar un origen común. Hay lenguas como el euskera que no tienen parentesco con el árbol genealógico de las lenguas indoeuropeas.
El problema, incluso diría el error, está en considerar que podemos hacer árboles filogenéticos basados en ciertas secuencias y no considerar que las bacterias pueden recibir aportes genéticos externos, normalmente plásmidos, transposones... y ese aporte genético les da unas peculiaridades patológicas que las convierten de hecho en especies nuevas. Da igual que el 99.9% de las secuencias genéticas cromosómicas sean similares. Con que una Salmonella, o un E. coli o Shigela (dicen que es un biotipo de E. coli) hayan adquirido genes de patogenicidad y éstos les abran el acceso a nuevos nichos ecológicos ésta nueva presión selectiva hará que se conviertan en especies nuevas. Por eso tradicionalmente a estos serotipos se les han denominado como especies.
Para entender los árboles familiares (filogenéticos) es muy útil emplear un simil linguístico como analogía. Por ejemplo, las lenguas romances como el francés, español, portugués, rumano proceden del latín. Si tomamos una palabra del latín original "factum" podemos ver como ha evolucionado a las palabras de los idiomas romances actuales
Las palabras van a tener un grado de identidad con la palabra "factum" de la cual proceden. Por ejemplo, el inglés tomó la palabra del latín recientemente por ese motivo hay muy poco cambio, de factum a fact. Si consideramos factum como el 100% de identidad, fact tiene 5 letras de las 6 letras originales. Cinco entre seis nos da un 83% de similitud. El castellano actual tiene 1 letra, la c en hecho, de seis de factum, uno dividido entre seis 17%.
Con esos datos, podemos concluir que la palabra fact está más cerca del latín que hecho. Utilizamos el porcentaje de similitud como un mapa. Si dos puntos tienen 17% de similitud, es lo mismo que decir 83% de distancia (100-17). La palabra hecho estaría un 83% alejada de factum. Dos puntos a tan solo 17% de distancia (100-83 similitud) como es el caso de factum y fact indicaría que estarían proximos.
En el caso de hecho, castellano actual, está más próxima a fecho, castellano antiguo, que a feito, palabra galego-portuguesa. De esta manera generamos, lo mismo que cuando comparamos las distancias entre distintas ciudades, un gráfico resumen de la distancia entre las palabras:
Con estas distancias se pueden construir árboles filogenéticos, que curiosamente se pueden superponer a mapas físicos:
Lo curioso es que los señor@s filogenetistas no contemplen que en cada uno de esos territorios hay una historia de mestizaje. Por ejemplo, a pesar de que el castellano deriva en su mayor parte del latín, no podemos hacer una historia genealógica común con el término izquierdo, que es de origen íbero. Tendríamos que remontarnos mucho más atrás, a las lenguas indoeuropeas para encontrar un origen común. Hay lenguas como el euskera que no tienen parentesco con el árbol genealógico de las lenguas indoeuropeas.
Evolución de la palabra dos, desde el idioma indoeuropeo "dwoh" hasta todas las formas actuales en los distintos idiomas que proceden del indoeuropeo. Nuestro idioma está formado por una estructura fonética lineal, que tiene su translación a la escritura. A medida que un idioma, pongamos por ejemplo un idioma ancestral del que derivan casi todos los idiomas europeos, estoy hablando del protoindoeuropeo, va expandiéndose y colonizando nuevos territorios, en estos nuevos territorios, con nuevas condiciones, de manera natural, algunas formas de pronunciar las antiguas palabras van teniendo más éxito y acaban por pronunciarse (y por lo tanto, escribirse) de manera diferente
¿Qué es el mestizaje en lingüística y genética?
El español que se habla en el Ecuador no procede 100% del español de España. Al llegar el idioma había en este país bastantes idiomas distintos, uno por cada comunidad, actualmente hay catalogadas unas 17. El idioma mayoritario era el kichwa y son multitud las palabras kichwas que existen en el español ecuatoriano. Asimismo, el español no es un idioma 100% derivado del latín. Tuvimos aporte muy importantes del árabe etc.
Esos nuevos aportes fuerzan la evolución de una manera particular. En Quito, los quiteños acaban muchas palabras en f: sif en vez de sif, quiteñof... la f final es una contracción del pues: si pues deriva en sif. En Chile ocurre algo similar con el po al final de las frases. Además, hay construcciones gramaticales que fuerzan nuevas combinaciones de palabras: "andarasme haciendo, ve" en donde se combinan tres verbos. La influencia del kichwa es obvia, y esto claro, influye en la particular evolución del castellano ecuatoriano o andino.
El mestizaje genético en las bacterias se da constantemente a través de incorporaciones de material genético de virus, plásmidos, transposones. Este material genético es egoísta. Tiene capacidad de imponer su criterio a la bacteria hospedadora ¿Cómo? la principal característica de este ADN externo vírico es que fuerza a la transmisión. La bacteria ahora ya nunca más será comensal, el virus la obliga a forzar su rápida transmisión.
Salmonella tiene dos islas de patogenicidad, antiguos transposones, insertados en su genoma. Uno tiene proteínas para modificar el comportamiento de macrófagos y la otra isla de patogenicidad tienen proteínas para modificar la respuesta inmunitaria del las células de los intestinos en donde viven las Salmonellas. Cada isla de patogenicidad codifica para unas jeringuillas bacterianas (los sistemas de secreción tipo III) para que la bacteria pueda repartir las proteínas víricas con las cuales va a hacer que: los macrófagos no las puedan comer y que a través de una inflamación controlada puedan provocar diarrea y penetrar en el cuerpo del hospedador.
Shigela, que hay quien dice que es un biotipo muy patogénico de E. coli, tiene un gran plásmido que controla también estos dos aspectos: evitar que los macrófagos los coman y poder jugar con el sistema inmune del hospedador en el marco de los intestinos.
Shigela está muy adaptada a los humanos, y cada vez que existe adaptación se van perdiendo funciones innecesarias. Con tan solo 100-200 células Shigela puede infectar humanos ¿Para qué va a necesitar flagelos siendo tan infectiva? por ese motivo, se han seleccionado cepas inmóviles que se transmiten igual de bien y además no gastan energía innecesaria fabricando flagelos. Salmonella necesita un millón de células para infectar a los humanos. Tiene flagelos. Por ese motivo, hay una diferencia entre Salmonella y Shigela, que Salmonella puede nadar "río arriba" a través del conducto cístico (ver figura abajo) y colonizar la vesícula biliar desde el intestino. Shigela no puede hacer esto por ser inmóvil.
Salmonella y Shigela hacen del intestino delgado, ya no su hogar, sino por fuerza de estos genes víricos que les obligan a transmitirse transmitirse y transmitirse, una plataforma de generar grandes números que se van a dispersar por los cursos de agua en forma de diarreas.
Hay innumerables ejemplos de ello. Wolbachia, una bacteria que cuando tiene determinados genes de origen plasmídico es capaz de invadir a los artrópodos y cambiar las frecuencias sexuales de toda la población. Wolbachia más virus genera un nuevo territorio, unas nuevas pautas infectivas y de colonización del hospedador. Ese nuevo territorio las convierte en especies nuevas.
El español que se habla en el Ecuador no procede 100% del español de España. Al llegar el idioma había en este país bastantes idiomas distintos, uno por cada comunidad, actualmente hay catalogadas unas 17. El idioma mayoritario era el kichwa y son multitud las palabras kichwas que existen en el español ecuatoriano. Asimismo, el español no es un idioma 100% derivado del latín. Tuvimos aporte muy importantes del árabe etc.
Esos nuevos aportes fuerzan la evolución de una manera particular. En Quito, los quiteños acaban muchas palabras en f: sif en vez de sif, quiteñof... la f final es una contracción del pues: si pues deriva en sif. En Chile ocurre algo similar con el po al final de las frases. Además, hay construcciones gramaticales que fuerzan nuevas combinaciones de palabras: "andarasme haciendo, ve" en donde se combinan tres verbos. La influencia del kichwa es obvia, y esto claro, influye en la particular evolución del castellano ecuatoriano o andino.
El mestizaje genético en las bacterias se da constantemente a través de incorporaciones de material genético de virus, plásmidos, transposones. Este material genético es egoísta. Tiene capacidad de imponer su criterio a la bacteria hospedadora ¿Cómo? la principal característica de este ADN externo vírico es que fuerza a la transmisión. La bacteria ahora ya nunca más será comensal, el virus la obliga a forzar su rápida transmisión.
Salmonella tiene dos islas de patogenicidad, antiguos transposones, insertados en su genoma. Uno tiene proteínas para modificar el comportamiento de macrófagos y la otra isla de patogenicidad tienen proteínas para modificar la respuesta inmunitaria del las células de los intestinos en donde viven las Salmonellas. Cada isla de patogenicidad codifica para unas jeringuillas bacterianas (los sistemas de secreción tipo III) para que la bacteria pueda repartir las proteínas víricas con las cuales va a hacer que: los macrófagos no las puedan comer y que a través de una inflamación controlada puedan provocar diarrea y penetrar en el cuerpo del hospedador.
Shigela, que hay quien dice que es un biotipo muy patogénico de E. coli, tiene un gran plásmido que controla también estos dos aspectos: evitar que los macrófagos los coman y poder jugar con el sistema inmune del hospedador en el marco de los intestinos.
 |
| Tejido linfoide asociado al tubo digestivo o GALT (gut-associated lymphoid tissue). Se compone de folículos linfoides a todo lo largo del tubo gastrointestinal casi todos están aislados entre si. Destacan las placas de Peyer, situadas en la lámina propia de la mucosa del intestino delgado. Tanto Salmonella como Shigela aprovechan las células M para penetrar en el interior del intestino delgado. |
Salmonella y Shigela hacen del intestino delgado, ya no su hogar, sino por fuerza de estos genes víricos que les obligan a transmitirse transmitirse y transmitirse, una plataforma de generar grandes números que se van a dispersar por los cursos de agua en forma de diarreas.
El plásmido vírico que tiene Shigela tiene una toxina citotóxica, la toxina Shiga, que hace que las diarreas provocadas por Shigela sean hemorrágicas. Salmonella no produce diarreas hemorrágicas.
Las Salmonellas o las Shigelas mestizas, con estos genes víricos, ya no son la bacteria original, por mucho que tengan un 99.99% de genes en común. Son especies distintas. Lo mismo que el español andino, que es un idioma con un sentir y una evolución propia. Los defensores de la fortaleza de la filogenia aducirán que es posible comunicarse entre un español de españa y un hablante de español andino. Es cierto. Las E. coli y Shigela comparten muchísimo ADN, lo mismo que los 2500 serotipos de Salmonella. Lo que las diferencia es el territorio que ocupan. El territorio marca un inicio evolutivo diferente.
 |
| Salasaca, Ecuador. Español, inglés y kichwa en el cartel de una panadería |
 |
| Fotografías tomadas en Salasaca, Ecuador. |
Referencia:
Marcos-Merino, José; Gallego, Rocío; Ochoa de Alda, Jesús. (2017). Introducción de la evolución molecular a través de una analogía lingüística. Libro de resúmenes: "II Workshop Estudiar Ciencias. Creando vocaciones científicas" ISSN: 2530-4925
miércoles, 18 de abril de 2018
H. influenzae y su vecino S. pneumoniae
H. influenzae fue la primera célula en ser secuenciado todo su genoma. Un genoma de 1.8 millones de pares de bases y sólo 1740 genes. Seis años después se publica el genoma de 2.0 millones de pares de bases de Streptococcus pneumoniae R6 que también vive, como H. influenzae en la parte superior del tracto respiratorio humano. Un año antes se secuenció Pseudomonas aeruginosa PA01, con 6.3 millones de pares de bases.
Cuantos más genes más ambiental es la bacteria. Las bacterias patógenas suelen sufrir una reducción del genoma. Es una evolución comprensible. Cuanto más patógeno menos cosas tienes que saber hacer. Sólo saber cómo extorsionar y vivir a cuenta del esfuerzo ajeno.
¿Cómo son las relaciones de vecindad entre H. influenzae y S. pneumoniae en la garganta?
Un estudio, publicado en 2005, puso en una placa de Petri a las dos bacterias para ver si competían. Lo que observaron es que S. pneumoniae siempre superaba a H. influenzae. La manera que tenía de dejar KO a H. influenzae era atacándolo con peróxido de hidrógeno.
Pero todos sabemos que las condiciones de una placa Petri no se parecen nada al hábitat natural de ambas bacterias, por ese motivo, los investigadores utilizaron ratones que, como mamíferos, son bastante parecidos a los humanos. A los pobres ratones les inocularon sus narices con ambas bacterias. Al cabo de dos semanas ¡Sorpresa! solo H. influenzae sobrevivía. Cuando se ponen por separado las dos sobreviven, faltaría más, les encanta el ambiente húmedo, caliente y rico en nutrientes de las gargantas de los mamíferos.
Al examinar el tejido fino respiratorio superior de los ratones expuestos a ambas especies de bacterias, se encontró un número extraordinariamente grande de células inmunes neutrófilas. En los ratones expuestos a solamente una de las bacterias, estas células no estaban presentes. Por lo tanto, parecía que los neutrófilos podían explicar porque H. influenzae desplazaba a S. pneumoniae de los ratones.
Cuando inoculaban con H. influenzae muertos al ratón, sus neutrófilos atacaban agresivamente a S. pneumoniae, mientras que cuando S. pneumoniae estaba sola en el ratón los neutrófilos no las atacaban. Sin embargo, los H. influenzae muertos no tenían ningún efecto en H. influenzae vivos.
Por ahora no hay todavía una buena explicación. Una podría ser que cuando S. pneumoniae ataca a H. influenzae, esto actúa como señal para que el sistema inmune ataque a S. pneumoniae.
La combinación de las dos especies acciona una respuesta del sistema inmune que no es disparada por cualquiera de las especies individualmente. El porqué H. influenzae no es afectado por la respuesta inmune se desconoce.
Fleischmann R, Adams M, White O, Clayton R, Kirkness E, Kerlavage A, Bult C, Tomb J, Dougherty B, Merrick J (1995). «Whole-genome random sequencing and assembly of Haemophilus influenzae Rd». Science 269 (5223): 496-512. PMID 7542800.
Cuantos más genes más ambiental es la bacteria. Las bacterias patógenas suelen sufrir una reducción del genoma. Es una evolución comprensible. Cuanto más patógeno menos cosas tienes que saber hacer. Sólo saber cómo extorsionar y vivir a cuenta del esfuerzo ajeno.
Breaking Bad - La evolución de Walter White. El profesor, padre de familia, trabajador a tiempo parcial en un lavado de carros se vuelve poco a poco en un criminal que gana harta plata sólo fabricando metaanfetamina y quitándose de en medio a los competidores
¿Cómo son las relaciones de vecindad entre H. influenzae y S. pneumoniae en la garganta?
Un estudio, publicado en 2005, puso en una placa de Petri a las dos bacterias para ver si competían. Lo que observaron es que S. pneumoniae siempre superaba a H. influenzae. La manera que tenía de dejar KO a H. influenzae era atacándolo con peróxido de hidrógeno.
Pero todos sabemos que las condiciones de una placa Petri no se parecen nada al hábitat natural de ambas bacterias, por ese motivo, los investigadores utilizaron ratones que, como mamíferos, son bastante parecidos a los humanos. A los pobres ratones les inocularon sus narices con ambas bacterias. Al cabo de dos semanas ¡Sorpresa! solo H. influenzae sobrevivía. Cuando se ponen por separado las dos sobreviven, faltaría más, les encanta el ambiente húmedo, caliente y rico en nutrientes de las gargantas de los mamíferos.
Al examinar el tejido fino respiratorio superior de los ratones expuestos a ambas especies de bacterias, se encontró un número extraordinariamente grande de células inmunes neutrófilas. En los ratones expuestos a solamente una de las bacterias, estas células no estaban presentes. Por lo tanto, parecía que los neutrófilos podían explicar porque H. influenzae desplazaba a S. pneumoniae de los ratones.
Cuando inoculaban con H. influenzae muertos al ratón, sus neutrófilos atacaban agresivamente a S. pneumoniae, mientras que cuando S. pneumoniae estaba sola en el ratón los neutrófilos no las atacaban. Sin embargo, los H. influenzae muertos no tenían ningún efecto en H. influenzae vivos.
Por ahora no hay todavía una buena explicación. Una podría ser que cuando S. pneumoniae ataca a H. influenzae, esto actúa como señal para que el sistema inmune ataque a S. pneumoniae.
La combinación de las dos especies acciona una respuesta del sistema inmune que no es disparada por cualquiera de las especies individualmente. El porqué H. influenzae no es afectado por la respuesta inmune se desconoce.
Referencia:
Lysenko E, Ratner A, Nelson A, Weiser J (2005). «The role of innate immune responses in the outcome of interspecies competition for colonization of mucosal surfaces». PLoS Pathog1 (1): e1. PMID 16201010.Fleischmann R, Adams M, White O, Clayton R, Kirkness E, Kerlavage A, Bult C, Tomb J, Dougherty B, Merrick J (1995). «Whole-genome random sequencing and assembly of Haemophilus influenzae Rd». Science 269 (5223): 496-512. PMID 7542800.
lunes, 16 de abril de 2018
Streptococcus agalactiae y su cápsula resbalosa
El factor de virulencia más importante de Streptococcus agalactiae es la cápsula de polisacáridos. Esta cápsula interfiere con la fagocitosis. Los macrófagos tienen problemas para atrapar a la bacteria que se comportaría como una pastilla de jabón. Estos problemas jabonosos duran hasta que el paciente desarrolla anticuerpos contra esta cápsula jabonosa. Por ese motivo, porque las personas pueden desarrollar anticuerpos contra cápsula, es que S. agalactiae causa problemas en recién nacidos. Si la madre no tiene anticuerpos, el recién nacido tiene riesgo de contraer la infección con esta bacteria. Por si fuera poco, cuando esta bacteria coloniza los genitales de la madre existe un mayor riesgo de parto prematuro y... los niños prematuros tienen mayor probabilidad de padecer la enfermedad.
domingo, 15 de abril de 2018
¿Qué función tiene el gen mecA?
El gen mecA codifica para proteína PBP2a que no es inhibida por la penicilina o la meticilina. Como no es inhibida por los antibióticos puede realizar tranquilamente su actividad transpeptidasa, es decir, que puede unir cadenas de peptidoglicano y así tupir la malla de peptidoglicano para que la presión interna de la célula no haga que ésta estalle.
viernes, 13 de abril de 2018
¿Curar pacientes es un modelo de negocio sostenible?
Extracto de Un mundo feliz de A. Huxley:
"Nuestro Ford (se refiere aquí el autor a Henry Ford, el industrial automovilístico de Detroit) hizo por su propia cuenta una enormidad para modificar el énfasis de la verdad y la belleza hacia la comodidad y la felicidad. La producción masiva exigía ese cambio. La felicidad universal mantiene las ruedas girando constantemente; la belleza y la verdad no pueden.Y, por supuesto, cuando llegó a ocurrir que las masas tomaban poder político, entonces era la felicidad lo que contaba y no lo la belleza y la verdad. Sin embargo, pese a todo, la investigación científica aún era permitida. Las personas aún seguían hablando de la belleza y la verdad como si fueran bienes soberanos. Hasta el tiempo de la Guerra de los Nueve Años. Eso hizo que cambiaran de tono completamente. ¿De que sirven la belleza o la verdad o el conocimiento cuando las bombas de anthrax están brotando por todas partes? En ese momento la ciencia empezó a ser controlada por primera vez... Las personas estaban listas hasta para que les controlaran sus apetitos. Todo por una vida tranquila. Hemos seguido controlando las cosas desde entonces. No fue muy bueno para la verdad, por supuesto. Pero ha sido muy bueno para la felicidad. Uno no puede tener algo gratis. La felicidad se debe de pagar".
No ha hecho falta esperar a una guerra bacteriológica para que el capitalismo se adueñe del conocimiento y la ciencia. Goldman Sachs, en un informe publicado por la empresa el 10 de abril de este años se plantea si curar pacientes es un negocio sostenible. Ver la noticia AQUÍ.
miércoles, 11 de abril de 2018
Ser buen profesor paga la pena
Hoy un alumno me enseñó algo que no sabía hacer. Fue emocionante. Qué él supiese resolverlo de esa manera me habló que en algún momento, aparte de la propia inteligencia del alumno, tuvo un buen profesor de matemáticas que supo explicar correctamente cómo se manejan los exponenciales. Algo que por lo visto, o bien yo no tuve, o bien carezco de la habilidad matemática para haberlo aprendido.
El problema que les puse fue el siguiente: tenemos 1 fragmento de ADN que queremos amplificar hasta 1 millón de copias. Si cada ciclo de PCR dura un minuto. ¿Cuánto tiempo pasará hasta que tengamos 1 millón de copias?
Yo cogí la calculadora y multipliqué de uno a dos y de dos a cuatro... y dándole 20 golpecitos al igual, cada golpecito 1 minuto, llegué a 1,048,576. Mi alumno lo resolvió elegantemente de la siguiente manera:
El problema que les puse fue el siguiente: tenemos 1 fragmento de ADN que queremos amplificar hasta 1 millón de copias. Si cada ciclo de PCR dura un minuto. ¿Cuánto tiempo pasará hasta que tengamos 1 millón de copias?
Yo cogí la calculadora y multipliqué de uno a dos y de dos a cuatro... y dándole 20 golpecitos al igual, cada golpecito 1 minuto, llegué a 1,048,576. Mi alumno lo resolvió elegantemente de la siguiente manera:
martes, 10 de abril de 2018
La quina en el Archivo de Indias de Sevilla
En el Archivo General de Indias de Sevilla se conserva un dibujo de los montes reservados para el cultivo de los árboles de la quina de 1769
 |
| Fotografía: Vianney Hidalgo |
 |
| Fotografía: Vianney Hidalgo |
lunes, 9 de abril de 2018
Hacer que llore Charles Darwin
Mi ojos sangraron al leer esta respuesta:
La pregunta es: Cuando aparecieron las bacterias aerobias ¿Qué ocurrió con las bacterias anaerobias?
La respuesta: "Las bacterias aerobias aparecieron cuando los mamíferos aparecieron en la tierra, es decir, es el origen de la vida terrenal, ya que antes era solo en el agua; las bacterias anaerobias siguen existiendo aún, en el caso de seres que viven en el agua, y en el ser humano, al hacer ejercicio usamos respiración anaerobia. Por lo tanto, aún siguen existiendo bacterias anaerobias, pero igualmente hay bacterias que se adaptaron".
Mira que les digo que las bacterias no se adaptan... se botan no más... no pues así
La pregunta es: Cuando aparecieron las bacterias aerobias ¿Qué ocurrió con las bacterias anaerobias?
La respuesta: "Las bacterias aerobias aparecieron cuando los mamíferos aparecieron en la tierra, es decir, es el origen de la vida terrenal, ya que antes era solo en el agua; las bacterias anaerobias siguen existiendo aún, en el caso de seres que viven en el agua, y en el ser humano, al hacer ejercicio usamos respiración anaerobia. Por lo tanto, aún siguen existiendo bacterias anaerobias, pero igualmente hay bacterias que se adaptaron".
Mira que les digo que las bacterias no se adaptan... se botan no más... no pues así
Los colores alucinantes de las bacterias
El biólogo sintético Tal Danino manipula bacterias en su laboratorio para crear patrones de colores alucinantes. Leer el artículo aquí
jueves, 5 de abril de 2018
Neisseria gonorrhoeae, el rey del disfraz
Esta bacteria va de dos en dos, por eso se llama diplococo (dos cocos). Se observa esa melenilla que es muy característica. Esos pelos, o fimbrias, le sirven para agarrarse a los epitelios, para intercambiar ADN, porque las fimbrias son huecas y pueden funcionar como penes bacterianos. Pero claro, son muy visibles y pueden ser reconocidos por las células del sistema inmune. Por ese motivo, N. gonorrhoea cambia la composición de sus pelos cada cierto tiempo. Es lo que se llama variación antigénica.
Los delincuentes hacen algo parecido. Por ejemplo, en la película "La Virgen de los sicarios" el sicario protagonista comete un crimen, da la vuelta a la esquina, se cambia la chompa y vuelve al lugar del crimen como si nada convencido de que nadie lo va a reconocer:
Cuando utilizamos analogías hay que ser muy cuidadoso porque en ciencia si hay algo que es necesario es el rigor, es decir, que lo que se dice se ajuste a lo que sabemos. Por ese motivo, en el siguiente video, a pesar de que la idea es buena, no se ajusta a la realidad:
martes, 3 de abril de 2018
Perros que dispersan bacterias resistentes a los antibióticos
En la Universidad de las Américas, con David Ortega, estamos realizando un trabajo sobre bacterias con resistencia a los antibióticos en las heces de perros que se encuentran en uno de los parques de Quito.
Hemos visto señales como la que se ve arriba intentando asustar con videovigilancia a los dueños de perros que no recogen las heces.
Cerca del parque Lineal de Quito acaban de abrir un macro hospital. La idea en el futuro será conocer si hay relación entre las bacterias de los parques y las que se encuentran dentro del hospital.
Nuestra sorpresa ha sido ver que en su día se habían instalado fundas de plástico gratuitas en el parque. La pena es que estos dispensarios de fundas estaban vacíos. Quizás sería buena idea que los policías que recorren el parque lleven fundas plásticas y que la ciudadanía sepa que ellos las tienen para que se las pidan.Existe carteles exhortando a los usuarios del parque a recoger los excrementos de sus perros.
Y aquí el autor del blog, vestido para la ocasión, buscando perritos para cogerlos "in fraganti".
lunes, 2 de abril de 2018
Tuberculosis, el precio de convivir con las vacas
El precio de beber leche
El ser humano es el único reservorio natural de Mycobacterium tuberculosis. Los estudios genéticos muestran que proviene de Mycobacterium bovis. ¿Cómo una bacteria patógena de vacas acabó especializándose en humanos? la razón es la domesticación. A fuerza de convivir con vacas, el M. bovis comenzó a infectarnos y la evolución seleccionó cepas que cada vez estaban más especializadas en humanos hasta que hoy en día tenemos dos especies diferentes M. tuberculosis y M. bovis
Los pueblos que domesticaron a las vacas adquirieron primero la tuberculosis. Cuando estos pueblos ganaderos se encontraron con otros pueblos que carecían de esta tecnología, obviamente mostraban una superioridad tecnológica y también inmunológica frente a esta enfermedad. De hecho, los pueblos no contactados suelen sufrir de altas tasas de tuberculosis cuando entran en contacto.
Mantoux o prueba de la tuberculina
El test de Mantoux es la prueba que consiste en inyectar antígenos purificados de Mycobacterium tuberculosis a una persona para comprobar si se ha producido contacto con Mycobacterium o con la vacuna BCG pero sin dejar huella.
Entre las 48 y las 96 horas se puede ya leer el resultado
El Quantiferon, o IGRA, tiene el mismo fundamento que el Mantoux con la diferencia de que el antígeno de TB (tuberculosis) empleado es específico de M. tuberculosis, por lo que evita los falsos positivos por micobacterias atípicas. No es una intradermorreacción. Del paciente se toma una muestra de sangre en tres tubos (neutro; con antígeno de M. tuberculosis, con mitógeno para detectar los casos de falso negativo por anergia, es decir por incapacidad de los linfocitos de reaccionar frente a un antígeno). El paciente que ha estado expuesto a TB y ha desarrollado una respuesta inmune va a tener circulantes LTh (CD4+) específicos capaces de reconocer el antígeno de TB e iniciar una respuesta de reclutamiento de células inmunitarias mediante la liberación de gamma interferón que es lo que se detecta mediante un ELISA.
Inhibición de la maduración del fagosoma: clave en el éxito como patógeno
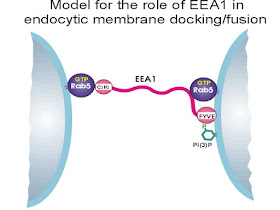
La proteína EEA1 se localiza exclusivamente en los endosomas tempranos y tiene un papel importante en el tráfico de endosomas. EEA1 se une directamente al PI-3-P, que es una proteína típica de la membrana plasmática, en su cara citoplasmática, lo hace por su extremo C-terminal, en el dominio FYVE y forma un homodímero
EEA1 actúa como una molécula de anclaje que se acopla a vesículas que portan SNAREs. Esto permite que los endosomas se acerquen el uno al otro y que, por último, se fusionen y el contenido del endosoma se entregue.
Además EEA1es un efector de RAB5A al cual se une vía un dedo de zinc en el N-terminal y esta unión es necesaria para la fusión de los endosomas tempranos y tardíos.
RAB5A se localiza en los endosomas tempranos donde está implicada en el reclutamiento de RAB7A y por tanto en la maduración de esos compartimentos en endosomas tardíos. Estas RABs permiten la maduración de los endosomas por ayudar al transporte de vacuolar (H+)-ATPasas (V-ATPasas) de la red Trans-Golgi a las vesículas endocíticas. Cuando estas ATPasas están en las vesículas van a acidificarlas, que es parte del proceso de maduración hasta que se fusionan con el lisosoma.
 |
| M. tuberculosis detiene la maduración del endosoma temprano antes de que se convierta en tardío y se fusione con el lisosoma |
M. tuberculosis impide la fusión del fagosoma con los lisosomas. Logra esta hazaña bloqueando la unión de EEA1, Legionella pneumophila hace algo parecido
Un tercio de la población mundial está infectada
La enfermedad es más frecuente en el Sudeste Asiático, África subsahariana y Europa del Este. Es curioso notar la alta prevalencia en la región andina. El estado de hacinamiento de las cárceles de la región, la altitud, el frío y que es una región extractivista en la que muchos obreros trabajan en minas sin la protección necesaria pueden servir de marco para entender esta alta tasa de infección.
 |
| Fuente: Data from World Health Organization. Global tuberculosis control: WHO report 2010. Geneva: World Health Organization; 2010. |
Dos millones de muertes
La diseminación a otras localizaciones ocurre fundamentalmente en pacientes inmunodeprimidos. Estudios calculan que M. tuberculosis es responsable de entre 1.5 y dos millones de muertes al año en el planeta, superando al SIDA como enfermedad infecciosa más letal. El problema, sin embargo, radica más en la pobreza que en otras causas.
Casos. En 2012 hubo 8,6 millones de nuevos infectados por tuberculosis. En 2000 eran 9 millones. La enfermedad tiene una forma pulmonar mayoritaria, pero hay otras (pleural, visceral, cerebral).
Exposición. Un 30% de la población mundial ha estado expuesta al bacilo de la tuberculosis, pero solo una pequeña parte desarrollará la enfermedad. Suelen ser personas vulnerables, por malnutrición o inmunodeficiencia.
Contagio. Para que haya contagio hace falta una exposición cercana a la persona infectada. El bacilo se transmite por el aire.
Mortalidad. Los tratamientos actuales son muy eficaces si se siguen bien. La tasa de mortalidad está en unas 12 de cada 100.000 personas. En 2012 fueron 1,3 millones, incluyendo 320.000 que también tenían VIH.
Países. 22 países reúnen el 80% de los casos. Los asiáticos (China, India, Indonesia, Filipinas... etcétera) representan el 60% de los casos. El resto se concentra en el sur de África y Brasil.
Vacuna bovina Calmette-Guerin
Se trata de una vacuna de Mycobacterium bovis cepa de Calmette-Guerin. Esta vacuna se recomienda de rutina en el momento del nacimiento en países de alta prevalencia de tuberculosis. Esta vacuna también se utiliza en la lepra y al ser inmunoestimulante, en el cancer de vejiga y en el melanoma.
¿Cómo te infectas de TB?
La tuberculosis se adquieres por la inhalación de partículas infecciosas en forma de aerosoles.
A los pacientes que eliminan bacilos en sus secreciones se les denomina "bacilíferos, son fuente de contagio y requieren aislamiento aéreo
 |
| Kohinur Begum, enferma de tuberculosis, con su hijo frente a su casa en un suburbio de Chittagong (Bangladesh). Fuente |
¿Pueden los bebes estar contagiados de tuberculosis?
Si. Se pueden contagiar de la madre por:Transmisión transplacentaria a través de la vena umbilical al hígado del feto o por aspiración o ingestión de líquido amniótico infectado. Los recien nacidos se pueden contagiar también por vía aérea procedente de contactos cercanos (familiares o personal de la sala de recién nacidos). Alrededor del 50% de los hijos de madres con tuberculosis pulmonar activa presentan la enfermedad durante el primer año de vida si no se indica quimioprofilaxis o vacuna BCG.
El granuloma, un ecosistema en donde infectar y reinfectar
La bacteria penetran en los macrófagos alveolares por fagocitosis y en ellos inhiben la acidificación del fagosoma y la posterior fusión del fagosoma-lisosoma, con lo que se replican libremente.
También los macrófagos circulantes y los linfocitos son atraídos hasta los focos de infección por los bacilos, restos celulares y factores quimiotácticos del hospedador. Se forman entonces las características células de Langerhans
Después de la tormenta llega la calma
Finalmente, según sea de exitosa la respuesta inmunitaria se conseguirá controlar la infección, o bien, se desarrollarán los síntomas clínicos. Alrededor del 60% de las personas infectadas van a desarrollar una forma latente asintómática que posteriormente puede reactivarse, generalmente asociado a una patología inmunosupresora, siendo el VIH la patología que más riesgo confiere de desarrollar una tuberculosis. En todos los pacientes que van a ser sometidos a un tratamiento inmunosupresor debe realizarse un screening de TB latente (prueba de la tuberculina).
Si tengo TB latente ¿Quiere decir que tengo M. tuberculosis en el cuerpo?
Si, aunque en muchas personas, la infección de tuberculosis latente nunca se convertirá en la enfermedad de tuberculosis. Pero algunas personas con la infección de tuberculosis latente tienen más probabilidades que otras de desarrollar la enfermedad de tuberculosis. Entre quienes tienen un riesgo alto se encuentran:
- Las personas con la infección por el VIH.
- Las personas que se infectaron por las bacterias de la tuberculosis en los últimos 2 años.
- Los bebés y los niños pequeños.
- Las personas que se inyectan drogas ilegales.
- Las personas que tienen otras enfermedades que debilitan el sistema inmunitario.
- Las personas de edad avanzada.
- Las personas que en el pasado no recibieron el tratamiento apropiado para la tuberculosis.
Cuadro clínico de TB en los pulmones
En el contexto de las primoinfección, localizándose a nivel pulmonar, y que en la mayoría de los casos cursa de forma subclínica y cura espontaneamente, pudiendo dejar un pequeño nódulo calcificado: lesión de Ghon
 |
| La flecha blanca señala la lesión de Ghon, un pequeño nódulo calcificado que se puede ver en radiografía. |
Varón de 35 años, preso en la Penitenciaría del Litoral, refiere que desde hace cuatro semanas ha venido padeciendo de sudoración profusa en la noche, perdida de apetito y fatiga.
Desde hace un mes y medio ha sufrido de tos con expectoración verdosa y hace dos días se volvió sanguinolenta. Ha bajado de peso y se alimenta menos.
Sin antecedentes patológicos personales.
T° 39°C. Paciente caquéctico. Pulmones: soplo tubárico y estertores en campo pulmonar derecho.
El cultivo de esputo evidenció bacilos alcohol-ácido resistentes fuertes, se espera resultados del cultivo que toman tres semanas.
Se inicia tratamientos con: isoniacida, pirazinamida, etambutol y rifampicina.