En el siglo XXI las enfermedades han dejado de tener un relato militar: el cuerpo humano luchando con su sistema inmune contra malvados patógenos que quieren hacernos daño. La realidad es más complicada. Lo que antes considerábamos como enemigo... ahora... debemos de ponernos en su piel y entender porqué tiene ese comportamiento patogénico. Es la manera de solucionar los problemas.
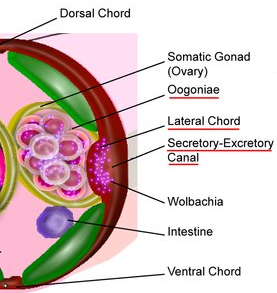
En este nuevo paradigma, entender que las especies involucradas son como matriuskas genéticas, es decir, un artrópodo con un gusano en su interior parasitado por una bacteria que tiene unas secuencias víricas que la empujan a un comportamiento egoísta y anómalo.
. Autora: Pierina Córdova
Hasta ahora se pensaba que la enfermedad estaba causada por gusanos parásitos que construyen túneles en la piel y liberan millones de larvas que se distribuyen por todo el cuerpo hasta provocar una reacción inmune que conlleva la inflamación de los ojos y, posteriormente, ceguera.
RESULTADOS:
1. ¿Por qué se considera Wolbachia un endosimbionte en O. volvulus en vez de un
parásito?
Endosimbiosis se refiere a la asociación de dos organismos, en la que uno habita en el interior
de otro organismo («Endosimbiosis», 2022). Un ejemplo de esto son los organismos eucarióticos
que son capaces de realizar procesos metabólicos originados en bacterias. Mientras que el
parasitismo se refiere a una asociación de dos organismos en las que el huésped se ve afectado por
el parásito, el cual vive a expensas y se beneficia de aquel organismo. Por lo tanto, al considerar
Wolbachia como un endosimbionte en lugar de un parásito en O. volvulus, es debido a que tienen
un papel esencial en la patogénesis de nemátodo. Un ejemplo de esta endosimbiosis es que las
especies que contienen Wolbachia inducen keratitis en el hospedador, mientras que aquellas
especies de O. volvulus tratadas con antibióticos para Wolbachia no inducen la inflamación de la
córnea. Además, Wolbachia proporciona procesos biológicos para O. volvulus, tal como la
biosíntesis de heme, riboflavina y nucleótidos como purina y pirimidinas. La bacteria es necesaria
para la reproducción y supervivencia del nemátodo. Por lo tanto, esta asociación es beneficial, más
no perjudicial, tanto para O. volvulus y Wolbachia.
2. ¿Mata la doxiciclina al parásito? ¿Qué efecto tiene este antibiótico en la cura de la
enfermedad de los ríos?
El antibiótico doxiciclina fue la primera droga utilizada como tratamiento para la oncocercosis
humana para eliminar Wolbachia. El efecto de este antibiótico es de eliminar Wolbachia mediante
la degeneración de ooquistes y las etapas embriogénicas tempranas (Kramer et al., 2018). La
doxiciclina mata a más del 60% de las bacterias hembras adultas, y disminuye la fertilidad de las
que sobreviven. Cabe recalcar, que el antibiótico no elimina a las microfilarias. Por lo tanto, al
eliminar el endosimbionte Wolbachia de O. volvulus este no inducirá la inflamación de la córnea,
lo cual llevaría al paciente a desarrollar la enfermedad de la ceguera de los ríos.
3. ¿Cuántas especies concurren en la enfermedad de la ceguera de los ríos? Explica el
papel de cada una en el proceso infectivo
La enfermedad de la ceguera de los ríos, o también llamada oncocercosis, su agente etiológico
es un nemátodo filarial, en específico la especie Onchocerca volvulus. Este parásito se disemina a
través de moscas negras, especies de Simulium, que se hallan comúnmente cerca de arroyos o ríos
que fluyen con gran rapidez. De hecho, un estudio de oncocercosis en el Ecuador reveló que las
especies de Simulium más comunes era S. quadrivitatum, seguido por S. esiguum y S. antillarum
(v98n2p117.pdf, s. f.).
En el ciclo vital participan tres especies. Primero, moscas negras (especies de Simulium); segundo,
Onchocerca volvulus y finalmente, el humano. Durante la ingestión de sangre, el humano sufre
varias picaduras por la mosca negra e introduce las filarias de O. volvulus dentro de la piel del
hospedador, el humano. Estas larvas se desarrollan en adultas, en la piel y tejido linfático. Esto
puede durar hasta 30 meses, mientras que en el caso de las hembras fecundas es de 15 años.
Luego, la mosca negra vuelva a picar al individuo, ingiriendo microfilarias a partir de la sangre.
Posteriormente, migran hacia los músculos torácicos de aquella especie donde se desarrollan en
larvas infectantes. Finalmente comienza nuevamente el ciclo con la picadura de la mosca negra al
humano (Onchocerca volvulus - Life Cycle, s. f.).
4. ¿Qué distribución tiene esta enfermedad y por qué? ¿A que es debido que tenga esa
distribución en específico y no sea una enfermedad que afecte a todo el mundo?
La distribución de esta enfermedad está caracterizada por regiones tropicales de América y
subsaharianas de África (Oncocercosis - «Ceguera de los ríos» - OPS/OMS | Organización
Panamericana de la Salud, s. f.). No es una enfermedad que afecta a nivel mundial, es endémica.
Esto se debe principalmente a que las larvas de la mosca negra, el vector de O. volvulus, se
reproducen en los alrededores de los ríos y arroyos con una corriente rápida. Por lo tanto, estos
sitios con la característica mencionada anteriormente suelen verse afectada con brotes o focos
pequeños de oncocercosis, como por ejemplo en Ecuador, Colombia, Venezuela, Guatemala,
Yemen, entre otros.
5. ¿Qué organismo internacional ha combatido la ceguera de los ríos en África? ¿Sería
posible erradicar una enfermedad exclusivamente con iniciativas de salud
nacionales? ¿Qué presidente de los EEUU retiró a su país de esta organización?
¿Por qué crees que un presidente como ese puede ser elegido democráticamente?
El organismo internacional que ha combatido la ceguera de los ríos en África es la
Organización Mundial de la Salud (OMS). Entre el año 1974 y 2009, el Programa de Lucha contra
la Oncocercosis fumigó contra las larvas de la mosca negra, junto con la distribución a gran escala
de ivermectina. Entre sus logros, consiguió prevenir la ceguera en 600,000 personas y evitar la
infección de 40 millones (Oncocercosis, s. f.). Las iniciativas de salud nacional sí son importantes
para erradicar una enfermedad. Sin embargo, los países afectados por esta enfermedad endémica
suelen ser de bajos recursos, por lo que se les dificulta el éxito de los programas de eliminación de
oncocercosis. Las organizaciones internacionales serían de gran contribución en el cumplimiento
de dicho objetivo.
El presidente de los EEUU que retiró al país de la Organización Mundial de la Salud, fue Donald
Trump. Este hecho sucedió en el año 2020, entre sus acusaciones mencionó que China presiona a
la OMS para “engañar al mundo” sobre el coronavirus. Sin embargo, no dio evidencias de aquello.
El republicano ganó las elecciones democráticamente en el año 2016, debido a que logró
sintonizar con las clases medias industriales, rurales, sin estudios universitarios, de ciudades
pequeñas de “América profunda”. Además, el 61.4% de la población estadounidense en edad de
votar informó haber votado, siendo mayor los simpatizantes de Trump (Bureau, s. f.). Quizás eso
fue un factor influyente en porqué el magnate consiguió la victoria.
6. ¿Cómo se eliminó O. volvulus del Ecuador? ¿Qué medidas se adoptaron? ¿Sería
importante recordar a la población que Ecuador ha sido el segundo país del mundo
en erradicar esta enfermedad? ¿Por qué?
En el año 2014, la Organización Panamericana de la Salud declaró a Ecuador un país libre de
oncocercosis. La medida que adoptaron fue la distribución masiva del fármaco ivermectina dos
veces al año durante el periodo de 1990 hasta 2009, en las poblaciones que se veían afectadas por
esta enfermedad, como en Esmeraldas (La OMS declara a Ecuador libre de oncocercosis, s. f.).
Además de la administración de medicina, se garantizó la educación en oncocercosis, atención
médica, desparasitación a menores de 5 años, vacunación, tomas de muestras, control de las
embarazadas, búsqueda de casos, entre otras medidas para asegurar una educación integral de la
población (Estudios confirman que está eliminada la oncocercosis en Ecuador – Ministerio de
Salud Pública, s. f.). Luego del tratamiento farmacológico, estas poblaciones estuvieron bajo
vigilancia epidemiológica durante tres años para confirmar la ausencia de transmisión del
patógeno. Posteriormente, el país solicitó a la OMS una verificación formal de la eliminación
mediante la visita de un equipo de expertos. Si es importante recordar que la población
ecuatoriana ha sido la segunda a nivel mundial en erradicar la oncocercosis, debido a que afecta a
más de 37 millones de personas. Por lo tanto, los líderes de los demás países con esta enfermedad
endémica pueden tomar iniciativa a partir de este logro y ejecutar las mismas medidas exitosas en
su país.
7. ¿Tiene la ceguera de los ríos pacientes asintomáticos? ¿Y paucisintomáticos?
Si, la ceguera de los ríos si tiene pacientes asintomáticos. De hecho, la mayoría de infectados
son asintomáticos. Esto se debe al hecho de que el parásito en su estado adulto puede vivir en el
humano hasta 15 años. Paucisintomático se define como “de la forma clínica con escasa y/o poco
expresiva sintomatología”. En la enfermedad de la ceguera de los ríos, pacientes
paucisintomáticos serían aquellos que presentan manifestaciones como fatiga, prurito, dolores
óseos y articulares. Luego, del otro extremo del espectro de la manifestación clínica se hallan los
pacientes con oncocercosis generalizada. Típicamente estos individuos presentan síntomas como
uveítis, atrofia del nervio óptico, oncocoriorrenititis (afectación de la retina), oncodermatitis
papular, oncocercomas (nódulos subcutáneos), entre otras afectaciones oculares, o cutáneos.
8. ¿Tiene esta enfermedad un reservorio animal? ¿Es importante este dato?
Según la Organización Panamericana de la Salud, el Reservorio animal se refiere a “cualquier
animal en donde normalmente vive y se multiplica un agente infeccioso, y del cual depende para
su supervivencia, y donde se reproduce de manera que pueda ser transmitido a un huésped
susceptible” (Taller sobre planificacion, administracion y evaluacion Glosario.pdf, s. f.).
En el caso de la oncocercosis, el reservorio animal son los seres humanos. En los nódulos del
hospedador es donde las larvas de O. volvulus se convierten en gusanos adultos. El apareamiento
de los gusanos puede producir 1000 micro filarias cada día. Estas formas inmaduras del gusano
suelen vivir en la piel y en los vasos linfáticos. Por lo tanto, el ser humano es el reservorio de la
especie hasta que esta sea transmitida nuevamente por la mosca negra hacia otro individuo
susceptible.
9. Las respuestas Th1 preferentemente se desarrollan durante las infecciones por
bacterias intracelulares, mientras las células Th2 predominan durante las
infestaciones por nemátodos gastrointestinales. ¿Hay cambios en las respuestas
Th1/Th2 en la enfermedad de la ceguera de los ríos? ¿A qué crees que son debidos?
Los linfocitos T colaboradores son un subgrupo de linfocitos que se encargan de la activación
del sistema inmune, mediante la secreción de citoquinas, para combatir los patógenos atacando al
hospedador. Se dividen en tres tipos; Th1, Th2 y Th17. Las Th1 son altamente efectivas en
eliminar patógenos intracelulares, las Th2 en erradicar helmintos, y finalmente las Th17 se
encargan de bacterias extracelulares y hongos. La bacteria intracelular Wolbachia es el principal
inductor de la inmunidad innata y adaptativa de Th1.
En la población existe tres subgrupos de infectados por O. volvulus: GEO (Generalized onchocercosis), Sowde (Severe chrome dermatitis), EN endemic normals
En los casos de oncocercosis generalizada, existen incrementos en los niveles de la respuesta de Th2, debido a la alta prevalencia dentro del hospedador de los nemátodos, sea en su estado adulto o microfilarial. En las personas Sowda aumenta mucho en una respuesta mediada por linfocitos Th2, a pesar de que sea inducido por un número bajo de filarias. En las personas endémicas normales (EN) infectadas la respuesta Th1/Th2 esta disminuida, mientras que después de tratamiento con ivermectina la respuesta se restaura parcialmente " In comparison to EN (small subgroup of people living in areas of endemicity do not acquire detectable patent infection despite exposure to infective vector bites), who show a mixed Th1/Th2 response, both responses appear to be downregulated in infected
people and partially restored after ivermectin (IVM) therapy" (Tamarozzi et al., 2011). Esta respuesta celular disminuida está asociada con la producción de IL-10, posterior al tratamiento con ivermectina la producción de la misma se redujo, permitiendo la proliferación celular (Hoerauf & Brattig, 2002).
Los cambios en la respuesta a la ceguera de los ríos dependen de la variabilidad genética de las poblaciones humanas.
10. ¿Qué papel cumple la sanidad pública en las enfermedades parasitarias?
Las enfermedades parasitarias constituyen un importante problema de salud pública a nivel
mundial, en especial países en vías de desarrollo. Por lo tanto, la sanidad pública debe intervenir
en las poblaciones, especialmente aquellas con alta prevalencia de parásitos. Un ejemplo de
intervención podría ser la desparasitación masiva, una o dos veces al año. Incluso, reforzar las
medidas de higiene personal, incremento al acceso de agua potable y saneamiento. Por lo que el
papel que cumple Salud Pública es de velar por la salud de las poblaciones, especialmente las más
vulnerables, monitoreando la prevalencia de las enfermedades y de sus microorganismos
patógenos, adoptando medidas en contra de ellas.
Bibliografía
Bureau, U. C. (s. f.). Voting in America: A Look at the 2016 Presidential Election. The United
States Census Bureau. Recuperado 28 de enero de 2022, de
https://www.census.gov/newsroom/blogs/random-samplings/2017/05/voting_in_america.
html
Endosimbiosis. (2022). En Wikipedia, la enciclopedia libre. https://es.wikipedia.org/w/index.php?
title=Endosimbiosis&oldid=141028242
Estudios confirman que está eliminada la oncocercosis en Ecuador – Ministerio de Salud Pública.
(s. f.). Recuperado 27 de enero de 2022, de https://www.salud.gob.ec/estudios-confirmanque-esta-eliminada-la-oncocercosis-en-ecuador/
Kramer, L., Crosara, S., Gnudi, G., Genchi, M., Mangia, C., Viglietti, A., & Quintavalla, C.
(2018). Wolbachia, doxycycline and macrocyclic lactones: New prospects in the
treatment of canine heartworm disease. Veterinary Parasitology, 254, 95-97.
https://doi.org/10.1016/j.vetpar.2018.03.005
La OMS declara a Ecuador libre de oncocercosis. (s. f.). ISGlobal. Recuperado 27 de enero de
2022, de https://www.isglobal.org/-/la-oms-declara-a-ecuador-libre-de-oncocercosis
Onchocerca volvulus—Life Cycle. (s. f.). Recuperado 27 de enero de 2022, de
https://www.mcdinternational.org/trainings/malaria/spanish/dpdx/HTML/Frames/A-F/
Filariasis/body_Filariasis_o_vol
Oncocercosis. (s. f.). Recuperado 28 de enero de 2022, de
https://www.who.int/es/news-room/fact-sheets/detail/onchocerciasis
Oncocercosis—"Ceguera de los ríos"—OPS/OMS | Organización Panamericana de la Salud.
(s. f.). Recuperado 27 de enero de 2022, de https://www.paho.org/es/temas/oncocercosisceguera-rios
Taller sobre planificacion, administracion y evaluacion Glosario.pdf. (s. f.). Recuperado 27 de
enero de 2022, de https://iris.paho.org/bitstream/handle/10665.2/3300/Taller%20sobre
%20planificacion%2C%20administracion%20y%20evaluacion%20Glosario.pdf?
sequence=1&isAllowed=y
Tamarozzi, F., Halliday, A., Gentil, K., Hoerauf, A., Pearlman, E., & Taylor, M. J. (2011). https://doi.org/10.1128/CMR.00057-10
V98n2p117.pdf. (s. f.). Recuperado 27 de enero de 2022, de
https://iris.paho.org/bitstream/handle/10665.2/16961/v98n2p117.pdf?
sequence=1&isAllowed=y